二氧化碳(CO2)的过度排放导致了全球变暖等严重的环境问题。其中,将CO2还原(CO2R)为高价值的化学品或燃料是解决该问题的一种最有希望的策略。目前,大量研究都集中在将CO2还原为气态产物(CH4、CO等)的贵金属催化剂。然而,由于其复杂的多电子反应过程,将CO2还原为液体燃料(甲醇、乙醇等)的选择性仍然较低。虽然通过高温破坏金属有机骨架(MOFs)结构而得到金属基纳米复合材料可广泛用作CO2RR光催化剂,但是被破坏的MOFs无法发挥其固有特性,导致选择性差、效率低或原子利用率低。近年来,具有独特电子结构和不饱和配位环境的单原子催化剂(SAs)被广泛的关注。SAs不仅可以暴露出丰富的活性催化位点和更高的原子使用率,而且可以提供一个原子尺度视角来理解光催化活性和结构特性之间的关系。因此,开发包含具有高气体吸附能力的原始MOF和具有原子水平的均匀金属活性位点的高效光催化剂,以实现CO2的有效转化,特别是对于获取具有高选择性的有价值液体燃料非常重要。


近日,清华大学王定胜教授和李亚栋院士、安徽师范大学毛俊杰教授等人报道了一种利用光诱导方法在UiO-66-NH2载体上锚定Cu单原子(Cu SAs/UiO-66-NH2),可以显着促进CO2转化为液态燃料。值得注意的是,在太阳光驱动下,制备的Cu SAs/UiO-66-NH2光催化CO2转化为甲醇和乙醇的转化速率分别为5.33和4.22 μmol h-1 g-1。该产率比初始UiO-66-NH2和Cu NPs/UiO-66-NH2复合物的产率高得多。通过密度泛函理论(DFT)计算表明,在UiO-66-NH2上引入Cu SAs可以极大地促进CO2向CHO*和CO*中间体的转化,从而能以极高的选择性生产甲醇和乙醇。该研究为设计原子级光催化CO2还原的高性能催化剂提供了新的见解。

制备与表征
如图1a所示合成路径,作者首先制备了Cu SAs/UiO-66-NH2光催化剂。通过透射电子显微镜(TEM)观察Cu SAs/UiO-66-NH2样品,未观察到存在Cu纳米颗粒。作者利用像差校正的高角度环形暗场扫描TEM(ACSTEM)测量,以验证UiO-66-NH2载体中Cu的形式。其中,红色圆圈标记的几个孤立亮点的原子分散被识别为Cu SAs。Cu SAs/UiO-66-NH2的元素映射图表明,Cu、C、N、O和Zr均匀分布在载体的整个骨架上。
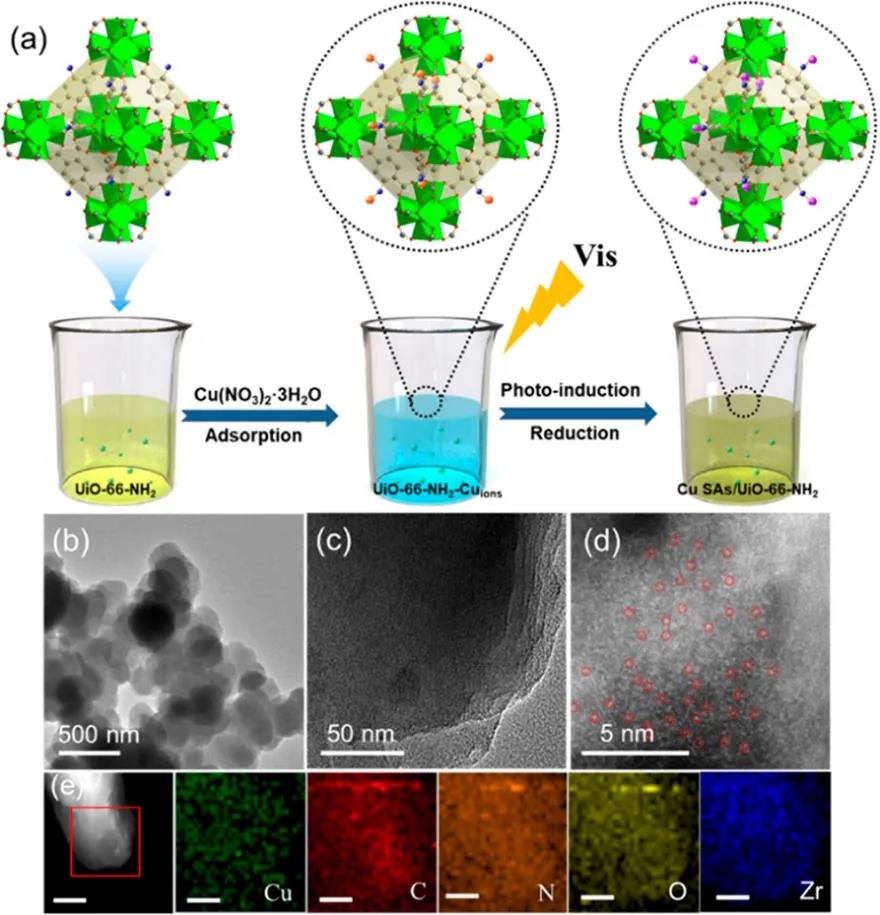
图1 Cu SAs/UiO-66-NH2的制备和表征
局部结构
作者利用元素选择性X射线吸收精细结构(XAFS)来进一步确认Cu SAs/UiO-66-NH2催化剂的局部配位结构。Cu SAs/UiO-66-NH2的吸收边缘位置位于Cu和CuO的吸收边缘位置间,表明Cu原子带正电且价态在0和+2之间。傅立叶变换扩展的X射线吸收精细结构(FT-EXAFS)光谱中,Cu SAs/UiO-66-NH2仅在1.50 Å处显示一个主峰,对应于Cu-N的第一个配位壳。Cu SAs/UiO-66-NH2的小波变换(WT)图显示,WT最大值在3.8 Å-1处。以上结果表明,在UiO-66-NH2基体中,分离出的Cu原子被锚定在原子水平上,并与两个N原子配位,原子距离为1.97 Å(Cu-N)。其局部原子结构模型如图2e所示。
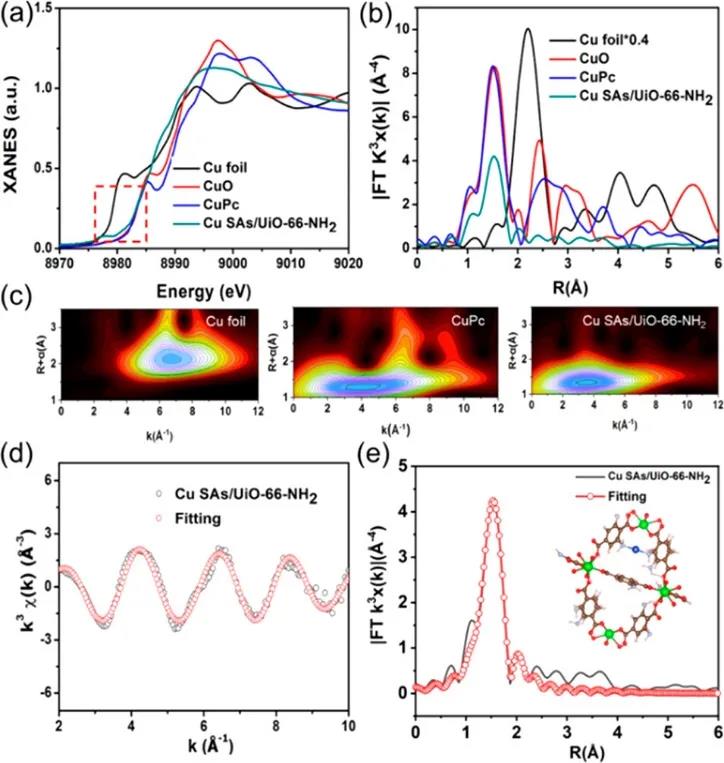
图2 Cu SAs/UiO-66-NH2的局部结构
催化性能
在可见光照射下,作者利用该催化剂在水溶液中进行光催化CO2还原。在Cu SAs/UiO-66-NH2存在下,发现液相产物只有甲醇和乙醇。其中,产生甲醇和乙醇的速率分别约为5.33和4.22 μmol h-1 g-1,远高于Cu NPs/UiO-66-NH2和初始UiO-66-NH2催化剂。记录时间分辨的光致发光(TRPL)光谱发现,对比UiO-66-NH2(τavg=4.91 ns),Cu SAs/UiO-66-NH2(τavg=6.53 ns)中光生电荷载流子的寿命显着延长。同时,对比Cu NPs/UiO-66-NH2和UiO-66-NH2,Cu SAs/UiO-66-NH2的光电流密度增加,表明在可见光照射下Cu SAs/UiO-66-NH2生成更多的载流子。Cu SAs/UiO-66-NH2的低温X波段EPR光谱表明,在可见光照射后Cu可以再生。在四次循环后,未观察到光催化活性的明显下降,确认了Cu SAs/UiO-66-NH2具有不错的稳定性。
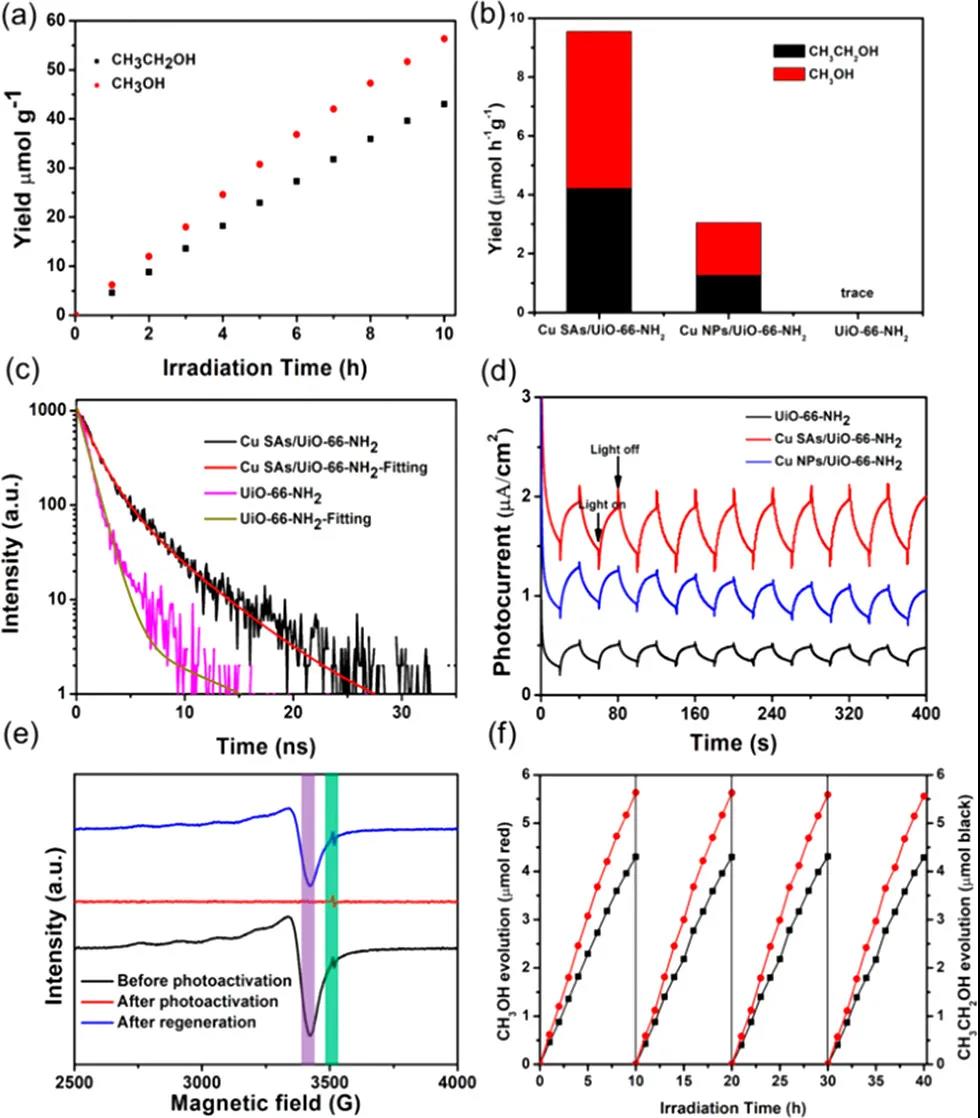
图3 Cu SAs/UiO-66-NH2的催化性能
催化机理
最后,作者利用密度泛函理论(DFT)计算检查了初始UiO-66-NH2和Cu SAs/UiO-66-NH2的电子结构。其中,图4a-c显示了计算出的状态总密度(TDOS)和局部状态密度(PDOS)。对比UiO-66-NH2的TDOS,在UiO-66-NH2中加入Cu SAs后,最高占据分子轨道(HOMO)和最低未占据分子轨道(LUMO)都向下以缩小带隙。Cu SAs/UiO-66-NH2的费米能级(Ef)也移至LUMO的底部,表明由复合材料中Cu SAs构型导致的电子迁移次数增加。在Cu SAs/UiO-66-NH2存在下,由于Cu的态密度(DOS)的重新分布,Cu位置处的COOH*和CHO*的形成能比其他催化剂小得多。需注意的是,CO*(源自*COOH)和CHO*(*CO加氢至*CHO)的形成可以很容易地在Cu位点进行偶联,有利于形成乙醇。对比Cu和Cu-CuO,Cu SAs/UiO-66-NH2上的自由能变化更有助于形成CO*和CHO*中间体,表明Cu SAs/UiO -66-NH2对CO*和CHO*中间体表现出更高的CO2还原活性。结果表明,UiO-66-NH2中的Cu SAs位点有助于形成CO*和CHO*,并且提高活性和光催化CO2还原为甲醇和乙醇的选择性。
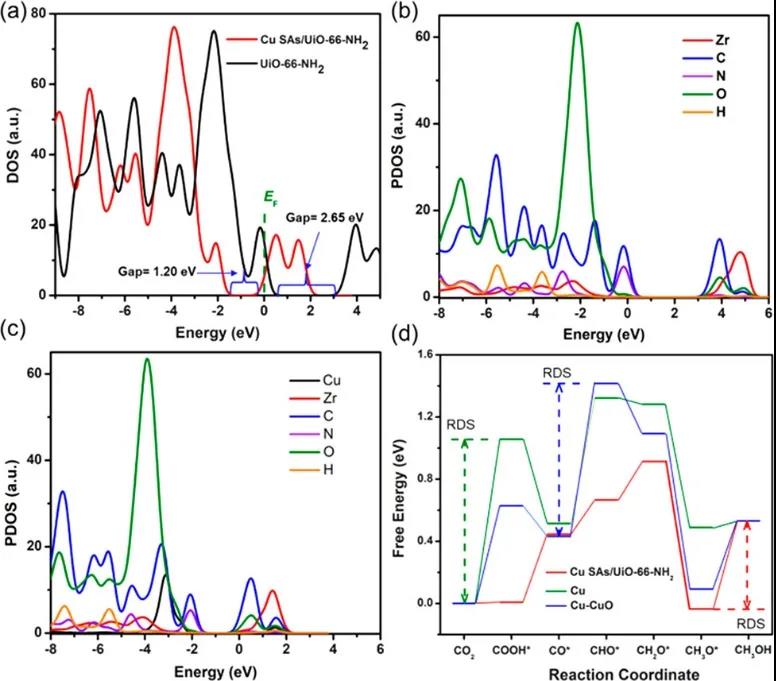
图4 Cu SAs/UiO-66-NH2的催化机理


Photoinduction of Cu Single Atoms Decorated on UiO-66-NH2 for Enhanced Photocatalytic Reduction of CO2 to Liquid Fuels. J. Am. Chem. Soc., 2020, DOI: 10.1021/jacs.0c09599.
免责声明:以上内容转自催化开天地。文章仅代表作者个人观点,不代表新威研选立场。