在持续和/或经济的分布式氨合成需求日益增长的刺激下,电化学氮还原反应引起了人们相当大的兴趣。然而,工业金属基氮还原反应催化剂中的含氮杂质,如金属氧化物和金属铁,却一直被忽视。
近日,来自美国乔治华盛顿大学的Stuart Licht & 威奇塔州立大学的Shuang Gu & 爱荷华州立大学的Wenzhen Li等研究者,从许多商业催化剂中发现,NOx−或氮化物中存在大量含氮物质。相关论文以题为“Revealing nitrogen-containing species in commercial catalysts used for ammonia electrosynthesis”于10月26日发表在Nature Catalysis上。



1. 研究者着重提出注意筛选商业催化剂中的NOx−/氮化物杂质的必要性,因为氮氧化物杂质通常不会在供应商的分析文件中列出。
2. 研究者推荐使用一种简单的两步程序(采用HPLC/ UV-vis分析后进行碱性/酸性处理)作为筛选催化剂材料中NOx−/氮化物杂质的可靠方法。
3. 此外,研究者对之前报道的具有15N-同位素标记和氮元素示踪的H2O-NaOH-KOH系统进行了实例分析,将电化学产生的NH3的真实氮源从气态N2重新分配为催化剂中的含氮杂质。


经过一个世纪的优化,Haber Bosch工艺已成为固定N2元素最成功的工艺。全世界的集中工厂每年合成约1.8亿公吨的人工NH3,随着化肥的广泛使用以提高农作物产量,这是20世纪人类文明最伟大的成就之一。由于N2稳定的化学性质,Haber Bosch工艺不仅需要高反应活性的苛刻条件(通常是300-500℃和150-250 bar),而且还需要分子H2和N2作为关键反应物。事实上,用于NH3合成的氢气生产在很大程度上依赖于化石燃料(主要是天然气)的改造,使用了全球大约1%的能源供应,占了总二氧化碳排放量的1-2%。由于人们对探索可持续发展的和/或经济的分布式氨合成越来越感兴趣,电化学和光化学方法已成为有前途的候选方法。
在过去的几年里,人们对理想的温和条件下的电催化氮还原反应(NRR)进行了大量的研究,金属基材料(如金属氧化物和金属合金)已经可通过不同的方法被用作NRR催化剂。然而,研究者们最近对产生NH3的真正来源提出了要求,并提出了一项严格的15N同位素标记方案供仔细检查。由于元素氮存在于已知的化学组成中,某些NRR催化剂的氮浸出,如金属氮化物,正被仔细研究;然而,用于NH3电合成的一般商业催化剂中含氮杂质的含量却被忽视了,这在很大程度上是由于主流化学品供应商长期以来对高质量化学品的信任。
此文中,鉴于金属氧化物和金属铁在不同NRR体系中制备催化材料中的频繁使用,研究者选择了一组材料作为分析的重点。研究者对其产品中含氮杂质的含量进行了仔细的检测。令人惊讶的是,在一些商业氧化物中检测到高水平的NO3-和NO2-离子(例如,在一个商业Bi2O3样品中,总NOx--N的含量为1,610±48 ppm),而在一个商业铁中,氮化物-N的含量高达7,297±99 ppm。


在工业金属氧化物中意外发现的氮氧化物杂质 在这里,研究者首先通过将催化剂样品浸泡在碱性溶液(0.1 M KOH)中提取NO2-和NO3-,然后使用配备紫外检测器的高效液相色谱分析浸泡溶液,对其进行量化(图1和2a等)。测定了商用Fe2O3中NO3-的氮含量为563 ±21 ppm。研究者对另外六种商业氧化物和其他供应商的六种铁氧化物中的NOx-含量进一步进行了量化。如图1所示,在13个氧化物样品中,有8个样品中含有可观水平的NO3-和/或NO2-杂质。通过0.1 M KOH溶液洗涤,氧化铁中的NO3−杂质可减少99%,或通过180℃热处理12小时可减少95%。
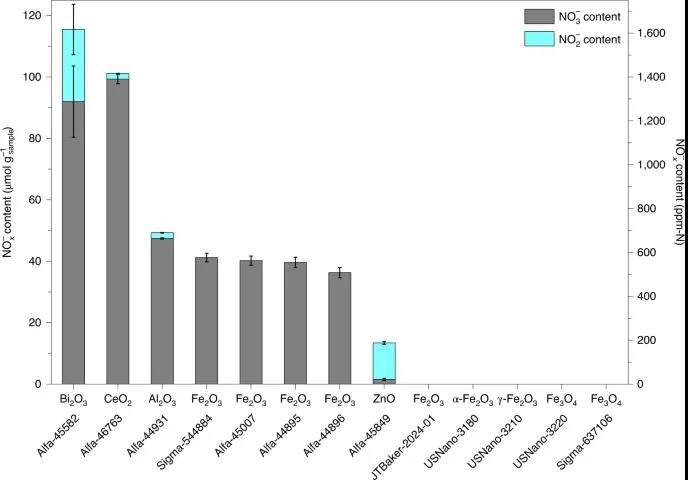
图1 在工业金属氧化物中检测到的杂质NOx−
除了从HPLC中测定出的NOx-杂质,研究者还通过TGA-MS分析直接观察到了NO——NO3−在热分解过程中形成的特征产物(图2b)。在150℃左右出现NO信号(m/z = 30),这与金属硝酸盐的分解温度吻合较好。
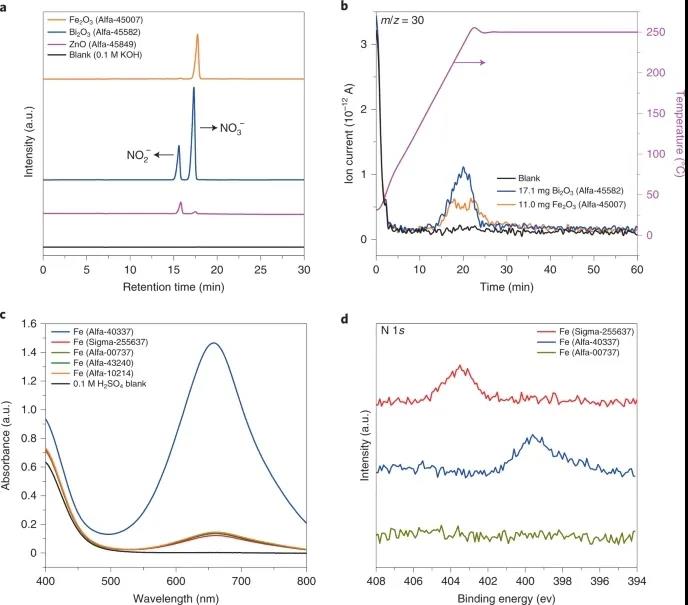
图2 在商业金属氧化物和金属铁中显示含氮杂质
在商业金属铁中意外的发现氮化物杂质。金属铁是工业生产纳米Fe2O3的前体,也是非均质N2固定的基准催化剂。研究者通过将五种商业铁产品溶解在0.1 M H2SO4(硝化氮被水解成NH4+)中,谨慎地检测了氮杂质,然后通过成熟的靛酚蓝比色法测定得到的溶液中NH4+的浓度。如图2c等所示,在所有五种铁样品溶液中都观察到了NH4+-N,可能来自氮化物。
需要指出的是,这些商品铁产品中氮化铁的化学成分各不相同。例如,研究者观察到独特的XPS氮1s信号:Alfa Aesar-40337 (7297 ppm-N)为399.6 eV, Sigma-Aldrich-255637为403.5 eV (391 ppm-N);图2d),即在与大块氮化物(~397 eV)相当的值下。氮1s峰位置的差异可能是由于与氮相连的氧原子数量不同,考虑到氮化铁表面暴露于氧时的硝基铵(NO+, 399-402 eV)和亚硝酸盐(NO2−,402.5-403.5 eV)的XPS信号。
H2O-NaOH-KOH系统案例分析。 研究者首先在含有40 wt%的水和等摩尔NaOH和KOH的H2O NaOH电解液中进行电解,温度为200℃,负载Fe2O3(Alfa Aesar no. 45007)催化剂。在恒定施加电流250 mA下,催化剂的总质量归一化铵生成量为39.2±1.3 ,非常接近HPLC测定的Alfa Aesar-45007中NO3−杂质的含量(563±21 ppm-N,相当于40.2±1.5 ),对应的总氮匹配平均为97.5%(图3a)。
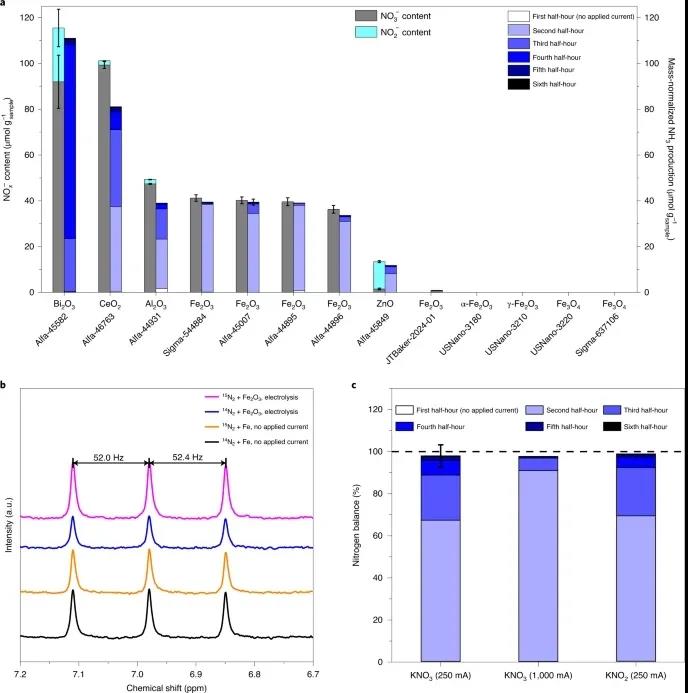
图3 H2O-NaOH-KOH体系中的电解
如参考文献所述,研究者重新评估H2O-NaOH-KOH电解液中的NRR。在系统中循环14N2和15N2两种情况下进行测试:(1)金属铁1克(Sigma-Aldrich no.255637)无电解电流12h;(2)在20、100、250、500、1000 mA(每个电流2.5 h)下用5 g Fe2O3洗涤电解。15N2循环实验均只检测到14NH4+,14NH3的累积代数在背景信号范围内下降(图3b)。15N标记实验的结果和元素氮的精确平衡与催化剂中发现的氮杂质高度一致,总的来说,电化学产生的NH3的真正来源应该从气态N2重新分配到Fe2O3催化剂中的含氮杂质。
筛选催化剂材料中氮氧化物杂质的建议。商业催化剂中NOx- /氮化物杂质的含量之高令人吃惊。值得注意的是,在长期的固氮历史中,研究人员周期性地受到氮污染问题的困扰和影响。除了在各种实验材料中观察到的含氮污染之外,在商业金属氧化物/金属铁中观察到的NOx−/氮化物杂质还提供了杂质鉴别的另一种解释,这些材料包括电解质、膜、喂养气体甚至丁腈手套。
当含氮材料参与催化剂的制备和处理时,实验室制造的催化剂也可能受到NOx−/氮化物杂质的筛选。因此,一种简单的两步程序被推荐为研究人员的可靠方案,因为该程序已被证明在定量金属氧化物和金属铁中的NOx−/氮化物杂质水平方面非常有效。
此外,研究者还建议报告(催化剂)质量标准化NH3生产,以及区域标准化NH3生产,以备将来研究之用。图4比较了铵电合成中报告的催化剂的质量和面积归一化铵产量。区域标准化NH3产量范围为三个数量级(从2×10−11到2×10−8 mol cm−2 s−1),质量标准化NH3产量范围为0.05到50 mmol g−1h−1);然而,区域标准化NH3生产并不总是与大规模标准化NH3生产一致。此外,报告质量标准化的NH3生产可能有助于比较不同方法的N2固定,以合理定位和评价体系的催化活性。
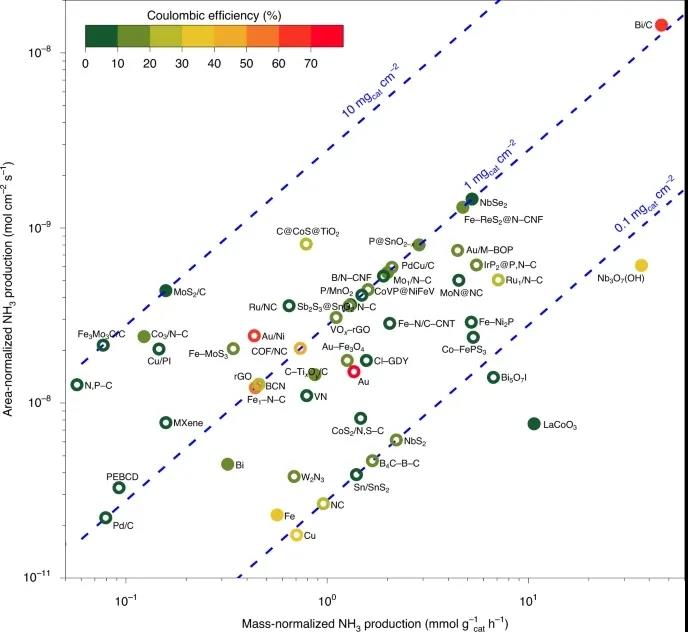
图4 报道的NRR电催化剂的面积和质量标准化NH3生产


综上,研究者从一些工业金属氧化物和金属铁中意外地发现了大量的NO3--N和含氮化合物。研究者推荐采用简单的两步程序(对 NOx−进行碱性处理或对氮化物进行酸性处理,然后采用HPLC或UV-vis分析)作为筛选催化剂材料中氮氧化物/氮化物杂质的可靠方案。研究者还建议在未来的研究中报告(催化剂)质量正化和(电极)区域正化NH3的生产。
H2O-NaOH-KOH体系虽然不能有效还原N2,但仍能以100%的选择性还原NOx-至NH3(图3c)。进一步探索容易的生物,生化,化学,光化学和电化学氧化N2 到NOx−可能开辟额外的生产途径,以低碳足迹从空气和水中生产NH3。


Chen, Y., Liu, H., Ha, N. et al. Revealing nitrogen-containing species in commercial catalysts used for ammonia electrosynthesis. Nat. Catal. (2020). https://doi.org/10.1038/s41929-020-00527-4
https://www.nature.com/articles/s41929-020-00527-4#citeas
免责声明:以上内容转自微算云平台。文章仅代表作者个人观点,不代表新威研选立场。